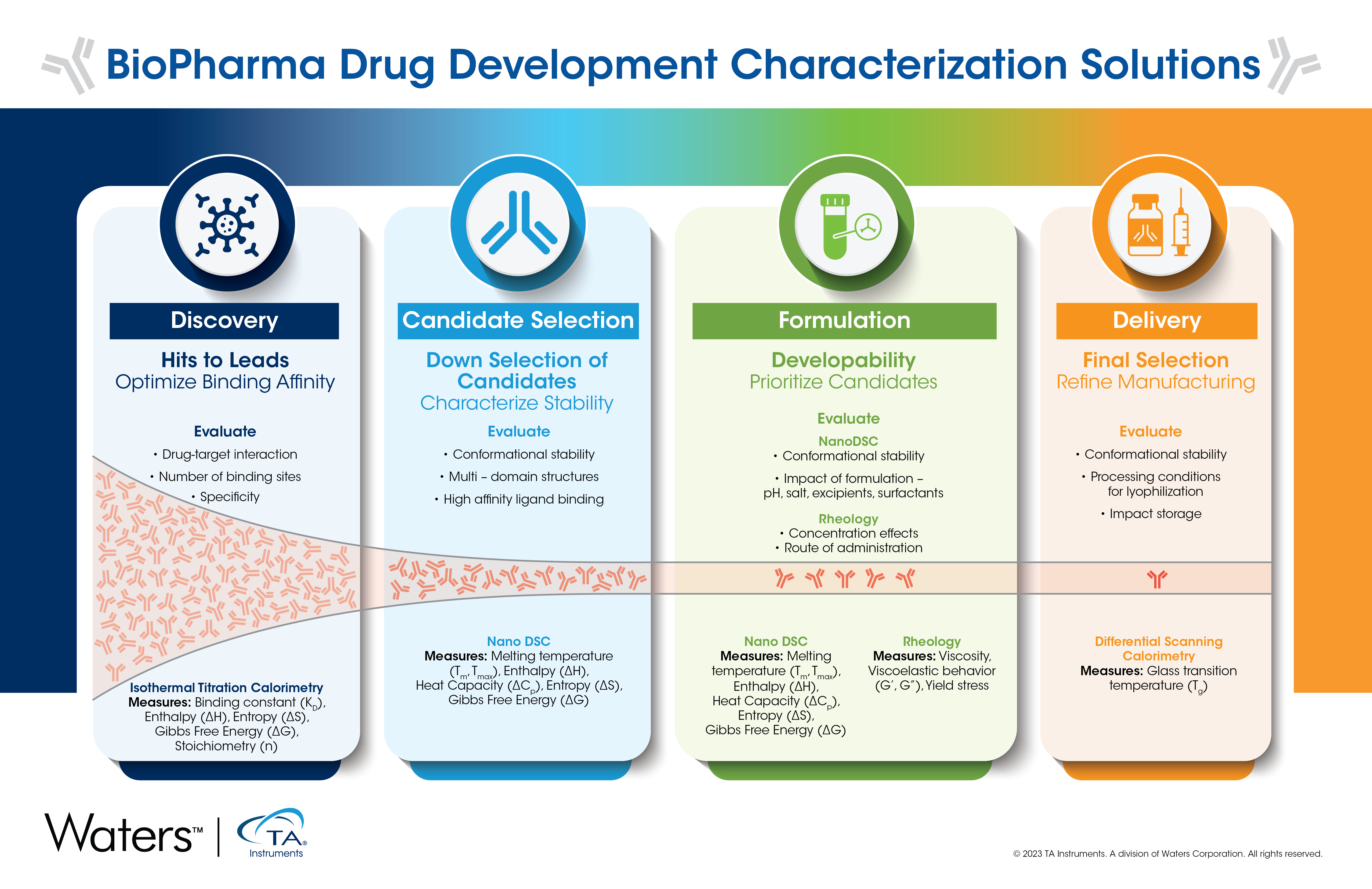
Flujo de trabajo y técnicas de desarrollo de fármacos BioPharma
Julienne Regele | Calliste Scholl | Morgan Ulrich
November 27, 2023
El desarrollo de fármacos es un proceso prolongado y complejo que comienza con el descubrimiento y, si tiene éxito, finaliza con la aprobación gubernamental para su comercialización. Cada paso en el proceso de desarrollo de fármacos, que se describe a continuación, tiene objetivos específicos con el objetivo de seleccionar resultados y candidatos apropiados para una sustancia farmacológica aprobada, y excluir los que sean inapropiados.
Aquí, analizamos los objetivos y técnicas relevantes utilizados en cada etapa del desarrollo de fármacos anticuerpos.
Descubrimiento
La fase de descubrimiento se divide en etapas temprana y tardía. El objetivo principal de las etapas de descubrimiento es eliminar cualquier secuencia con un desempeño no deseado, al considerar tanto las inestabilidades químicas como la unión al elemento de acción. El descubrimiento comenzará con un panel de anticuerpos grande que puede variar de cientos a miles, y que posteriormente se reduce a un fondo común de decenas. Para reducir el panel, la detección mediante simulación computacional (in silico) se utiliza comúnmente como una herramienta primaria porque en esta etapa la disponibilidad de muestras es muy escasa. En la detección in silico se utilizan simulaciones por computadora o herramientas de detección virtuales para hacer predicciones acerca del comportamiento de diferentes moléculas.1 La secuencia se analiza para minimizar el riesgo de cualquier “punto problemático” que pudiera interferir con la capacidad de desarrollo más adelante en el proceso. Una vez que se ha reducido el fondo común, se caracteriza la unión al antígeno para asegurar que el anticuerpo se una al elemento de acción identificado y se logre también la potencia deseada, de nuevo con el objetivo principal de reducir el número de anticuerpos que se van a caracterizar más.
Preformulación
En esta etapa, el número de anticuerpos se ha reducido a decenas durante el proceso de selección de los anticuerpos apropiados y exclusión de los inapropiados. Durante la preformulación, es importante asegurar que las pruebas se realicen en condiciones estables, lo que significa que puede ser necesario cierto nivel de selección de amortiguador. Tenga en cuenta que este amortiguador probablemente diferirá del amortiguador de formulación final. Tiene importancia caracterizar por completo los anticuerpos restantes comenzando con la validación de los estudios de unión realizados en etapas iniciales con calorimetría de titulación isotérmica (isothermal titration calorimetry, ITC).
La ITC es un método sin etiquetas y sin inmovilización para caracterizar interacciones de unión. Es una técnica rica en información que no sólo indica si algo se une, sino también las fuerzas impulsoras detrás de la interacción. Para cualquier terapéutica, es importante comprender plenamente cómo interactúa con el elemento de acción, incluso la especificidad o qué tan específica es la terapéutica para el elemento de acción. Asegurar especificidad alta dará por resultado una terapéutica con menos efectos secundarios no deseados causados por la unión fuera del el elemento de acción. Otros atributos importantes a caracterizar en esta etapa son la estabilidad conformacional, la estabilidad coloidal, la potencia y la estabilidad en el plasma. Esta información se utilizará en combinación para eliminar cualquier anticuerpo no deseado.3
Selección de candidatos
La fase de selección de candidatos se centra en evaluar los anticuerpos más promisorios para uso terapéutico. Las técnicas que se utilizan en esta sección exigen concentraciones que abarcan un rango más amplio de hasta 100 mg/ml, y se recopilarán tipos similares de información, como la estabilidad conformacional y la estabilidad coloidal; sin embargo, esta etapa requiere datos de resolución más alta. La estabilidad conformacional se evaluará al caracterizar tanto la Tinicio como TM, al utilizar calorimetría diferencial de barrido (differential scanning calorimetry, DSC).
La DSC Nano automatizada permite a los investigadores caracterizar la estabilidad a corto plazo de sus muestras sin el uso de etiquetas o colorantes exógenos, lo que simplifica así los flujos de trabajo y disminuye los errores en el desarrollo biofarmacéutico.2 Dentro de un experimento, los investigadores pueden determinar la temperatura de fusión, la entalpía y cambio de capacidad calorífica, lo que les permite calcular la energía libre para tomar una decisión plenamente informada sobre qué formulación es más estable.2 Esta determinación eficiente facilita el proceso de selección de candidatos. Además, también se completarán la caracterización fisicoquímica, la FC/PD in vivo y la evaluación de excipiente.
Formulación
Una vez que se seleccionan uno o dos anticuerpos, la investigación pasa a centrarse en optimizar la formulación final para los primeros ensayos en seres humanos. La estabilidad conformacional sigue siendo un atributo crucial para medir y vigilar por medio de este proceso de formulación. Se crea una serie de formulaciones al variar el pH, la sal, los azúcares y los surfactantes. Es probable que cada combinación cambie la estabilidad conformacional, de modo que es fundamental medir la estabilidad. A diferencia de algunas de las otras etapas, es importante realizar pruebas sobre la dosificación final de anticuerpos, que podría ser de hasta 200+ mg/ml. La técnica más valiosa para las pruebas de estabilidad es la DSC, que proporciona mediciones de estabilidad precisas para comparar diferentes formulaciones para ver cuál tiene el mayor potencial de desarrollabilidad.2
Entrega
Otra área clave a considerar durante la formulación y/o el proceso de formulación comercial es el modo de entrega. El modo de entrega influirá en la dosificación final y la forma final del producto, líquido o liofilizado. Los dos métodos de entrega más comunes para las formulaciones de fármacos anticuerpos son las inyecciones subcutáneas estables líquidas o las soluciones liofilizadas y reconstituidas para infusión intravenosa.4 Si la formulación se liofiliza para mejorar la vida útil, las condiciones bajo las cuales liofilizar se pueden entender mejor al determinar la temperatura de transición vítrea o temperatura de colapso.5 Durante el paso de secado primario, es fundamental diseñar una rampa de temperatura que se mantenga por debajo de esta temperatura a fin de evitar el colapso o la disminución de volumen de la estructura. La calorimetría diferencial de barrido (differential scanning calorimetry, DSC) es el estándar y la herramienta preferida para comprender esta información.
Microcalorímetros de vanguardia para el desarrollo acelerado de fármacos
Si bien el proceso de desarrollo de fármacos es prolongado y laborioso, TA Instruments proporciona soluciones eficientes y fáciles de usar para facilitar la investigación, el desarrollo y la fabricación. TA colabora estrechamente con nuestros clientes para determinar la mejor solución que se ajuste al propósito de cada uno de los hitos del desarrollo de fármacos. Nuestra gama de equipos de microcalorimetría está diseñada específicamente para crecer con las necesidades de investigación de usted, con la capacidad de agregar muestreo automático en cualquier momento. Además, la larga trayectoria de equipos sensibles de TA Instruments asegura datos creíbles y confiables.
Referencias
- In silico pharmacology for drug discovery: Methods for virtual ligand screening and profiling—PMC. (n.d.). Retrieved October 20, 2023, from https://www.ncbi.nlm.nih.gov/pmc/articles/PMC1978274/
- Nano DSC – TA Instruments. (2023, March 19). https://www.tainstruments.com/nanodsc/
- Affinity ITC – TA Instruments. (n.d.). Retrieved October 20, 2023, from https://www.tainstruments.com/affinity-itc-auto/
- Belissa, E., Vallet, T., Laribe-Caget, S., Chevallier, A., Chedhomme, F.-X., Abdallah, F., Bachalat, N., Belbachir, S.-A., Boulaich, I., Bloch, V., Delahaye, A., Depoisson, M., Wojcicki, A. D., Gibaud, S., Grancher, A.-S., Guinot, C., Lachuer, C., Lechowski, L., Leglise, P., … Boudy, V. (2019). Acceptability of oral liquid pharmaceutical products in older adults: Palatability and swallowability issues. BMC Geriatrics, 19(1), 344. https://doi.org/10.1186/s12877-019-1337-2
- Affairs, O. of R. (2022). Lyophilization of Parenteral (7/93). FDA. https://www.fda.gov/inspections-compliance-enforcement-and-criminal-investigations/inspection-guides/lyophilization-parenteral-793
Otros recursos
- Nota de aplicación – Characterizing Virus Structure and Binding
- Nota de aplicación – Characterizing Protein – Protein Interactions by ITC
- Nota de aplicación – Characterization of Biopharmaceutical Stability
- Nota de aplicación – Advances in Native Binding Assays
- Nota de aplicación – Determining Thermal Stability of Antibodies with a Nano DSC
- Nota de aplicación – A Novel Thermodynamic Assay for Predicting and Monitoring Biomolecular Structure Stability
- Seminario web – Biophysical Characterization of Antibodies in a Suspension: Solutions for Slurries
- Seminario web – Biophysical Characterization of Antibody Drug Conjugates Using DSC
- Instrumento – Nano DSC
- Instrumento – Isothermal Titration Calorimeters (ITC)
- Instrumento – Isothermal Microcalorimeters
- Contacto – Póngase en contacto con TA Instruments hoy