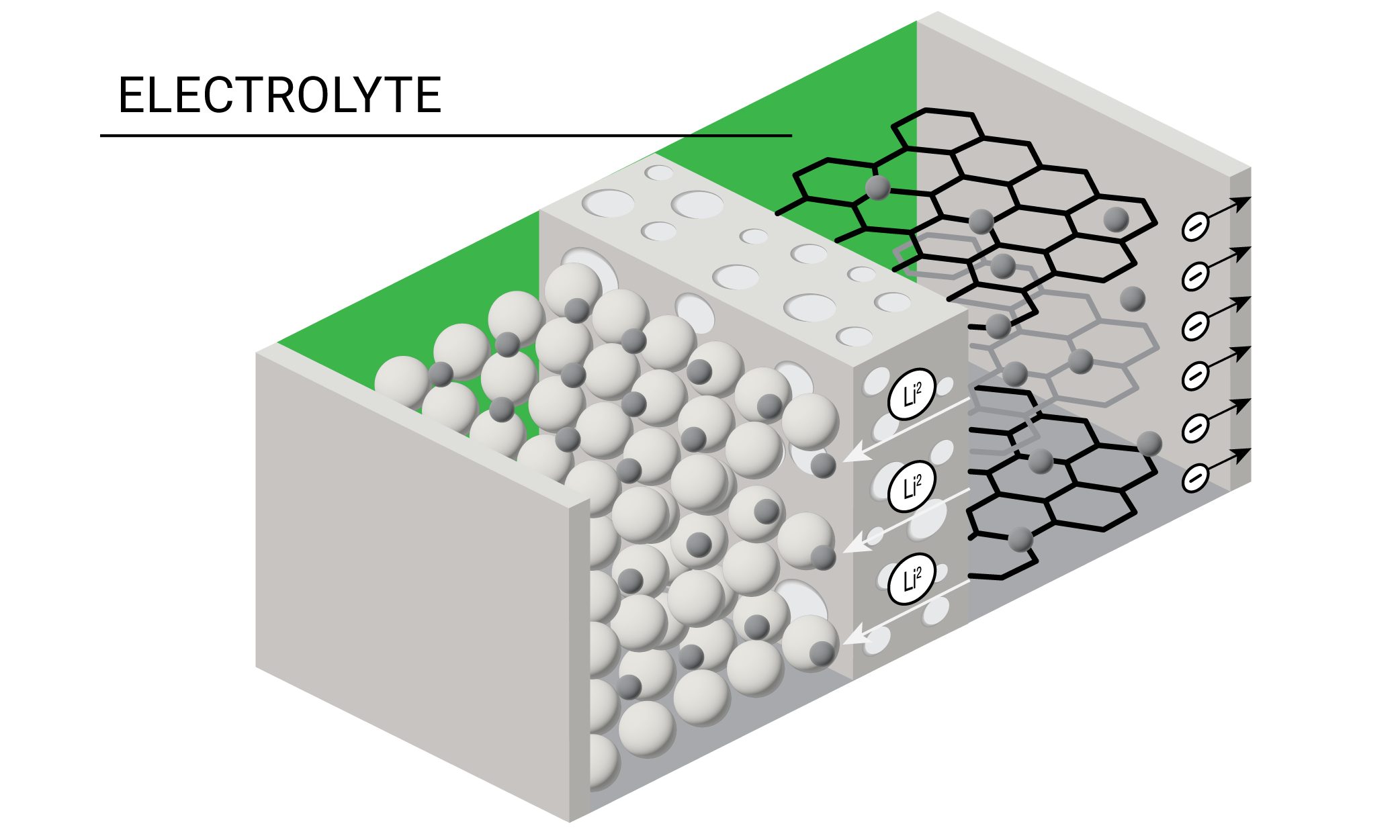
最關鍵的電池元件之一是電解液,也就是在放電過程中把帶正電的離子從陰極輸送到陽極的導電溶液。鋰離子電池的電解液傳統上是由溶解在有機溶劑混合物中的鋰鹽製成。在製造電池過程中,電解液的溶劑和鹽成分在陽極還原,產生固體電解質界面膜(SEI),在電池運行和安全方面扮演了關鍵的角色。
現今的電池研究人員正在試驗不同配方的液體、凝膠、聚合物和固態電解質。設計成功的電解液需要考慮平衡黏度、導電性、電化學穩定性和成本。大多數的電解液在低溫下表現優異,但即使在中等溫度下熱穩定性就有侷限。
電池開發商依靠熱分析來測量電解液的熱穩定性,確保設計可以避免退化和潛在的失火。可用差示掃描量熱法(DSC)和熱重分析(TGA)研究電解液的熱穩定性,對電解液的熱學性能提供全面分析。流變儀可使工程師測量黏度,並在製造過程中生產具有最佳泵送性的電解質溶劑。
儀器和測試參數
材料: 非水性溶劑
材料範例: 碳酸鹽和電解液、六氟磷酸鋰(LiPF6)
電解質與添加劑的分子降解
- 可泵送性、輸送
- 屈伏應力
- 黏度 (牛頓、切變稀化、切變增稠)
- 黏彈性
- 充電放電循環對傳導率的影響
- 黏度
- 電流變
- 大氣分析
- 可用手套箱操作
- 充滿氬氣與氮氣的環境
應用範例
哪些熱事件會導致熱失控?
雖然對電池的熱失控過程仍有待解的問題,但是目前的理解顯示它是由以下一系列事件引發的:隨著電池溫度不斷升高,導致熱失控的放熱反應與鋰離子電池(LIB)的每個內部元件發生破壞性的相互作用;其中一些元素率先被破壞,而大多數元素在失效時會使熱量加速累積。
第一個開始分解的元件是固體電解質界面膜(SEI),通常在 80-120°C(176-248°F)左右開始分解。此時可以減緩熱失控,但是一旦陽極暴露在電解液中,就不再可逆。在反應性陽極表面發生的放熱反應增加系統的熱量,直到下一個臨界溫度。
隔離膜是下一個受影響的元件,其失效有兩個階段:隔離膜在 120-150°C(248-302°F)左右開始熔化並造成小規模短路,然後在 220-250°C(428-482°F)左右破裂,造成更嚴重的內部短路。
以下反應會在前一個溫度範圍之後迅速直接地發生;陰極材料、黏著劑和電解液都開始分解,使電池芯的溫度急劇升到約 800°C(1472°F)。這些反應會產生氣體,增加 LIB 內的壓力。
第一個開始分解的元件是固體電解質界面膜(SEI),通常在 80-120°C(176-248°F)左右開始分解。此時可以減緩熱失控,但是一旦陽極暴露在電解液中,就不再可逆。在反應性陽極表面發生的放熱反應增加系統的熱量,直到下一個臨界溫度。
隔離膜是下一個受影響的元件,其失效有兩個階段:隔離膜在 120-150°C(248-302°F)左右開始熔化並造成小規模短路,然後在 220-250°C(428-482°F)左右破裂,造成更嚴重的內部短路。
以下反應會在前一個溫度範圍之後迅速直接地發生;陰極材料、黏著劑和電解液都開始分解,使電池芯的溫度急劇升到約 800°C(1472°F)。這些反應會產生氣體,增加 LIB 內的壓力。
TGA Thermogram Highlighting Thermal Instability of Graphite Anode Material
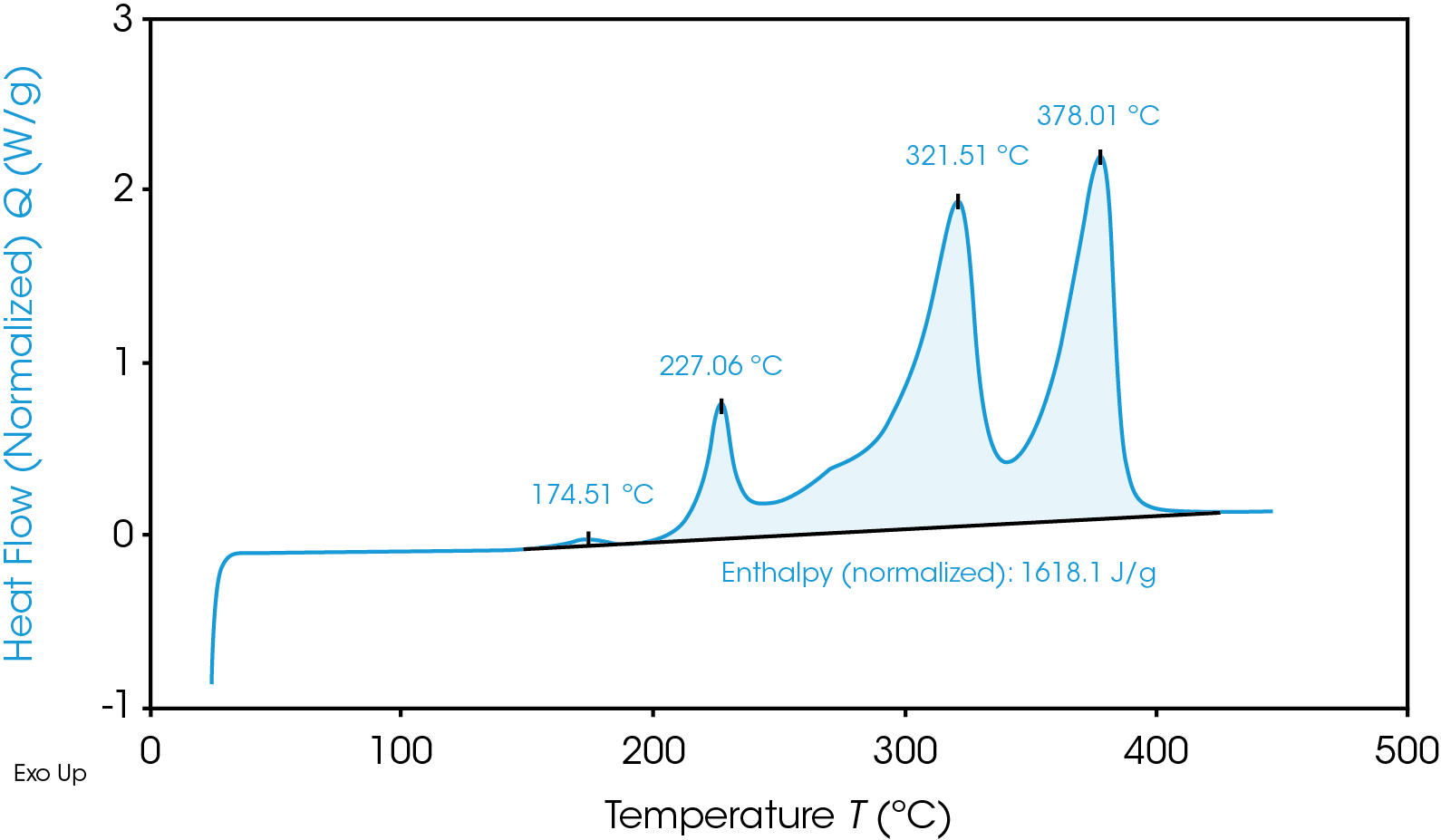
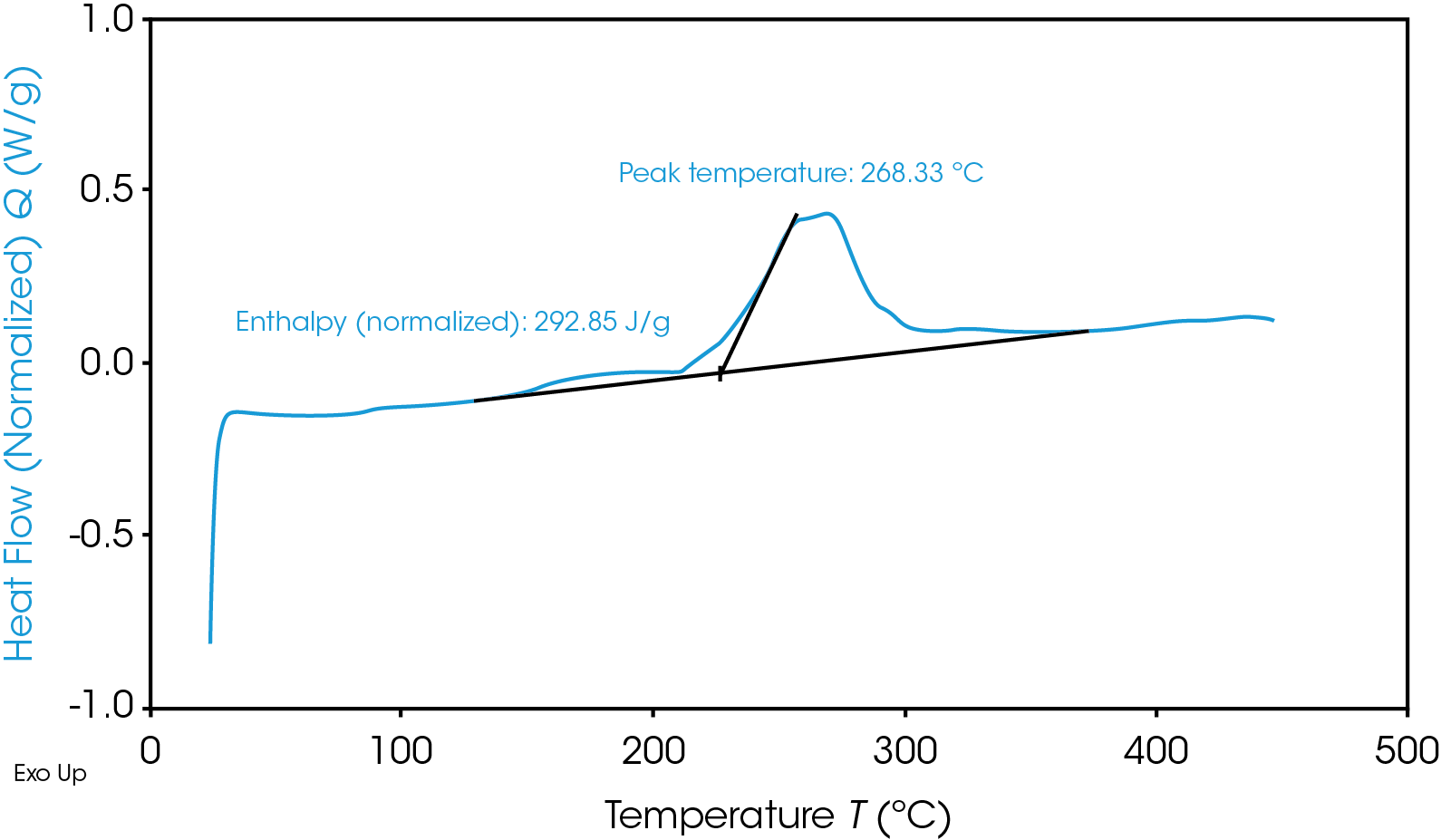
除了快速發熱外,陰極反應還有一個災難性的副產品,那就是易燃的氧氣。根據具體條件,直接的結果是「熱 + 氧氣 = 失火」或「熱 + 氣體 = 破裂/爆炸」。當然,所有材料都不盡相同,而且可能在這些溫度範圍內或是更高或更低,未來甚至在這些溫度之外,所以必須採用適當的測試為特定的電池選擇最安全的材料。
為了避免熱失控並選擇耐熱性最佳的電池材料,電池研究人員會進行差示掃描量熱法(DSC)和熱重分析(TGA):DSC:DSC 測量進入或流出材料的熱流,作為溫度或時間的函數。相變化打斷了溫度變化與吸收或釋放熱量之間的熱容量關係,可見於圖表Y軸。從安全操作溫度到熱濫用,它可在各種條件下進行測試。
TGA:TGA 測量樣品質量,作為溫度或時間的函數。一般來說,熱穩定性較好的材料可在質量變化之前達到較高的溫度。
使用 DSC 的測量結果回答下列問題:
- 材料的熔化溫度,Tm
- 材料的玻璃轉化溫度,Tg
- 構成電池的各種材料的最低相變溫度。
使用 TGA 的結果回答下列問題:
- 材料開始分解的溫度。
- 在給定溫度下,因熱分解或氧化分解而損失的樣品質量。
- 在給定溫度下的分解反應(包括氧化反應和熱誘導反應)速度。
- 構成電池的各種材料的最大熱穩定溫度。





