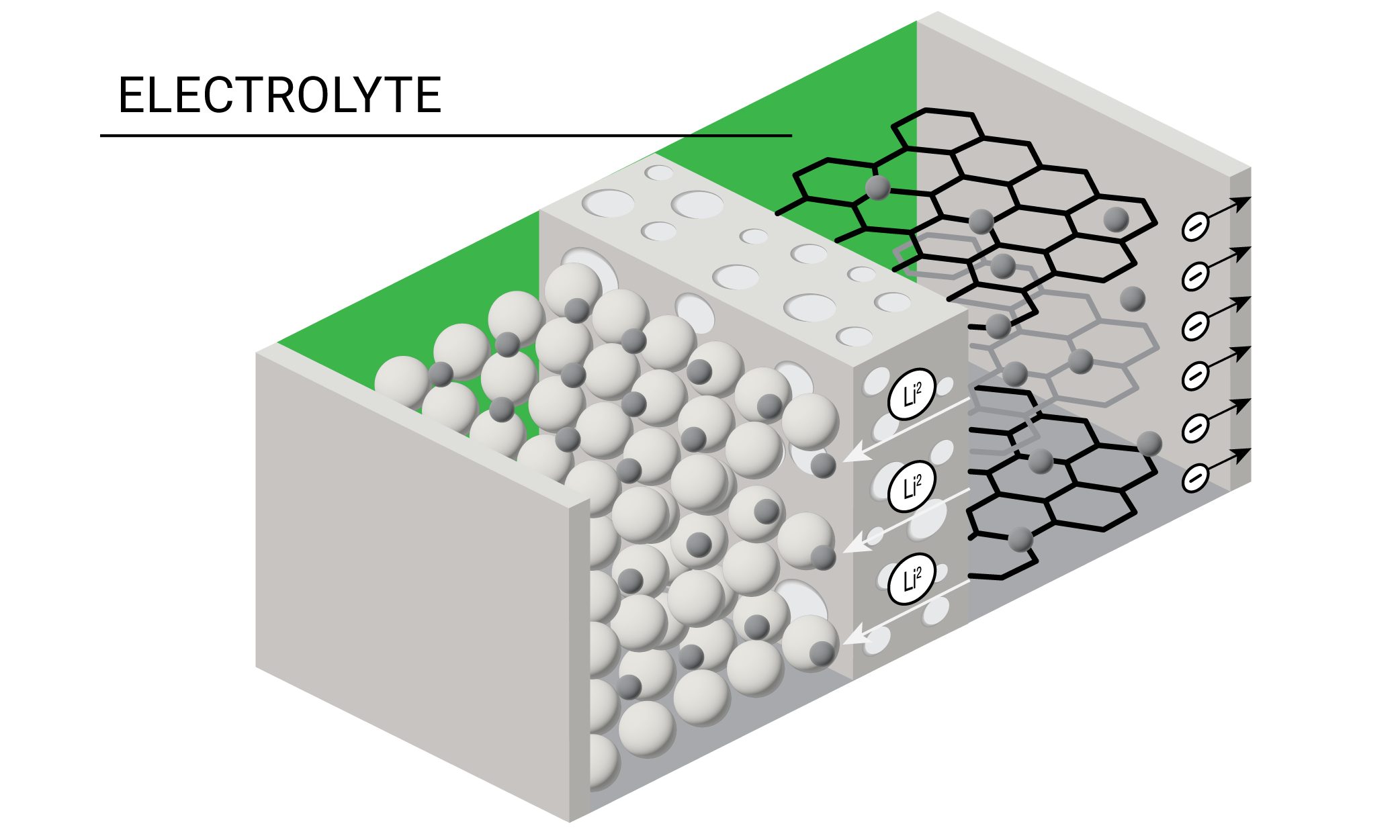
가장 중요한 배터리 구성 요소 중 하나는 방전 과정 중에 양으로 하전된 이온을 캐소드에서 애노드로 운반하는 전도성 용액인 전해질이다. 리튬 이온 배터리 전해질은 전통적으로 유기 용제 혼합물에 용해된 리튬 염으로 만들어진다. 배터리 배열 중에 전해질의 용제와 염 성분은 애노드에서 환원되어 배터리 작동과 안전에 중요한 역할을 하는 SEI(고체 전해질 계면상)를 생성한다.
오늘날의 배터리 연구자들은 액체, 젤, 폴리머, 고상 전해질의 다양한 제형을 실험하고 있다. 성공적인 전해질을 설계하려면 점도, 전도도, 전기화학적 안정성, 비용의 균형을 맞춰야 한다. 대부분의 전해질은 저온에서 잘 작동하지만 중간 정도의 온도에서도 열 안정성이 제한적이다.
배터리 개발자는 열 분석에 의존하여 전해질의 열 안정성을 측정하고 성능 저하와 잠재적 화재 위험을 방지하도록 설계해야 한다. 전해질 열 안정성은 DSC(시차 주사 열량 측정법)와 TGA(열중량 분석)로 조사할 수 있으며, 이러한 방법을 함께 사용하면 전해질의 열 특성을 포괄적으로 분석할 수 있다. 엔지니어는 유변학을 활용해 점도를 측정하고 제조 중 최적의 펌프 송출 능력으로 전해질 용제를 생산할 수 있다.
계측기 및 테스트 매개 변수
재료: 비수성 용제
재료의 예: 탄산염 및 전해액, 육불화인산리튬(LiPF6)
전해질과 첨가제의 분자 분해
- 열 안정성
- 분해 온도
- 조성 측정
- 휘발성 성분 함량
- 불순물 확인
- EGA(방출 기체 분석), TGA-MS, TGA-FTIR, TGA-GCMS
- 대기분석
- 글로브박스 작업 호환 가능
- 아르곤 및 질소 퍼지 환경
- 펌프 압송성, 운송성
- 항복 응력
- 점도(Newtonian, shear thinning, shear thickening)
- 점탄성
- 전도도에 대한 충전-방전 주기의 영향
- 점도
- ER(전기 – 유변물성)
- 대기분석
- 글로브박스 작업 호환 가능
- 아르곤 및 질소 퍼지 환경
응용 사례
열폭주로 이어지는 열 이벤트는 무엇일까?
배터리의 열폭주 과정에 대해 남아있는 의문이 있지만, 현재까지 파악한 바로는 다음과 같은 일련의 이벤트에 의해 열폭주가 시작되는 것으로 보인다. 열폭주로 이어지는 발열 반응은 배터리 온도가 계속 상승함에 따라 리튬 이온 배터리(LIB)의 모든 내부 구성 요소와 파괴적으로 상호 작용한다. 일부 요소는 초기에 피해를 입지만, 대부분의 요소는 고장을 일으키면서 열 축적을 직접 가속화한다.
맨 처음 파손되기 시작하는 구성 요소는 일반적으로 약 80~120°C(176~248°F)에서 문제가 시작되는 SEI(Solid-Electrolyte Interphase, 고체 전해질 계면상)이다. 이 시점에서 열폭주가 느려질 수 있지만 애노드가 일단 전해질에 노출되고 나면 더 이상 되돌릴 수 없다. 반응성 애노드 표면에서 발생하는 발열 반응으로 다음 임계 온도에 도달할 때까지 시스템에 더 많은 열이 가해진다.
그다음으로 영향을 받는 구성 요소는 분리막으로, 두 단계에서 정상 작동에 실패한다. 약 120~150°C(248~302°F)에서 분리막이 녹기 시작하여 작은 단락이 발생하고, 이어 220~250°C(428~482°F) 근처에서 분리막이 분해되면 더 심각한 내부 단락이 발생한다.
다음 반응은 이전 온도 범위에 따라 빠르고 직접적으로 발생하는데, 캐소드 재료, 바인더, 전해질이 모두 분해되기 시작하여 배터리 셀의 온도가 약 800°C(1,472°F)까지 급격히 상승한다. 이러한 반응에는 LIB 내의 압력을 증가시키는 가스 생성물이 있다.
맨 처음 파손되기 시작하는 구성 요소는 일반적으로 약 80~120°C(176~248°F)에서 문제가 시작되는 SEI(Solid-Electrolyte Interphase, 고체 전해질 계면상)이다. 이 시점에서 열폭주가 느려질 수 있지만 애노드가 일단 전해질에 노출되고 나면 더 이상 되돌릴 수 없다. 반응성 애노드 표면에서 발생하는 발열 반응으로 다음 임계 온도에 도달할 때까지 시스템에 더 많은 열이 가해진다.
그다음으로 영향을 받는 구성 요소는 분리막으로, 두 단계에서 정상 작동에 실패한다. 약 120~150°C(248~302°F)에서 분리막이 녹기 시작하여 작은 단락이 발생하고, 이어 220~250°C(428~482°F) 근처에서 분리막이 분해되면 더 심각한 내부 단락이 발생한다.
다음 반응은 이전 온도 범위에 따라 빠르고 직접적으로 발생하는데, 캐소드 재료, 바인더, 전해질이 모두 분해되기 시작하여 배터리 셀의 온도가 약 800°C(1,472°F)까지 급격히 상승한다. 이러한 반응에는 LIB 내의 압력을 증가시키는 가스 생성물이 있다.
흑연 애노드 재료의 열 불안정성을 강조 표시한 TGA 온도 기록도
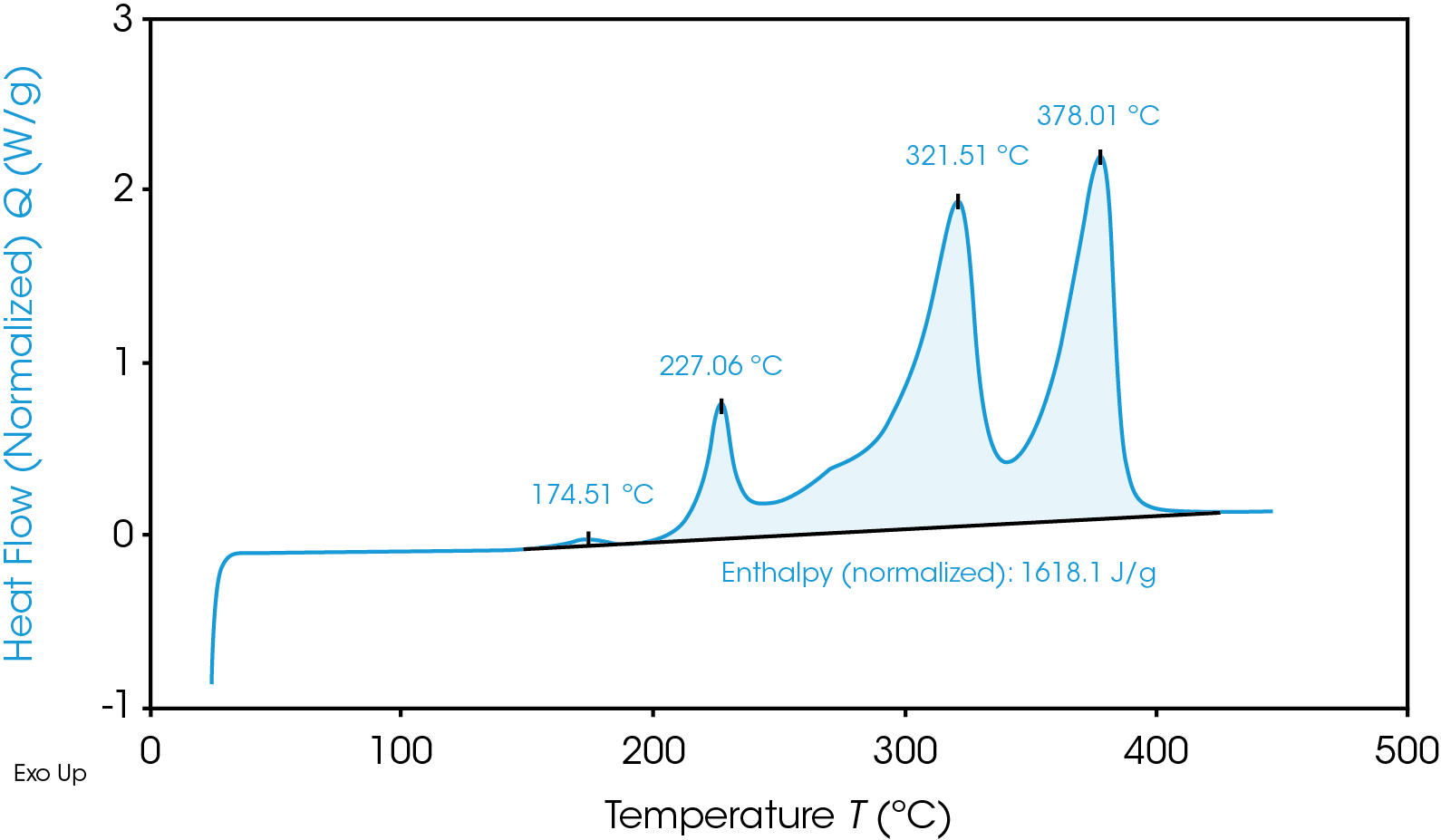
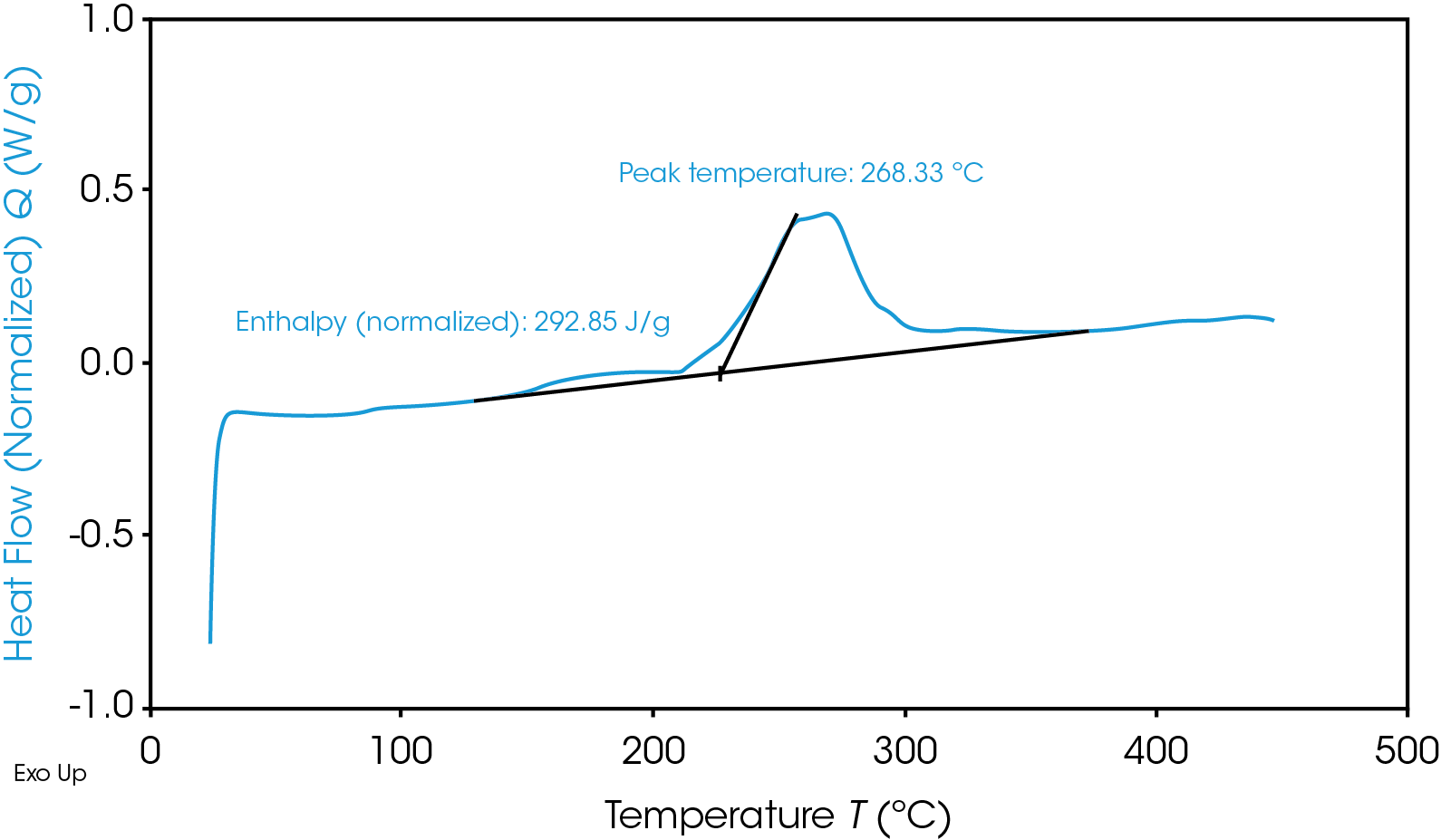
빠른 열 생성과는 별개로 캐소드 반응은 재앙적인 부산물로 가연성 산소를 생성한다. 정확한 조건에 따라, 그 즉각적인 결과는 “열 + 산소 = 화재” 또는 “열 + 가스 = 파열/폭발”이다. 물론, 모든 재료가 똑같이 만들어지는 것은 아니며 이러한 범위보다 다소 높거나 낮은 온도, 심지어 미래에는 이러한 온도를 벗어나 문제가 발생할 수도 있다. 따라서 적절한 테스트를 통해 해당 배터리를 위해 가능한 가장 안전한 재료를 선택하는 것이 필수적이다.
열폭주를 피하고 최적의 열 내성을 가진 배터리 재료를 선택하기 위해, 배터리 연구원들은 시차 주사 열량 측정법(DSC) 및 열중량 분석(TGA) 기술을 선택한다.
DSC: DSC는 재료로 들어오거나 재료에서 나가는 열류를 온도 또는 시간의 함수로 측정한다. 그래프 출력에서 볼 수 있는 상변화 발생 시 온도 변화와 흡수되거나 방출되는 열 사이의 열용량 관계가 중단된다. 안전한 작동 온도부터 열 남용까지의 다양한 조건에서 테스트할 수 있다.
TGA: TGA는 온도 또는 시간의 함수로 샘플의 질량을 측정한다. 일반적으로 말하자면, 열 안정성이 더 높은 재료는 더 높은 온도에 도달한 후에 질량 변화가 발생한다.
열폭주를 피하고 최적의 열 내성을 가진 배터리 재료를 선택하기 위해, 배터리 연구원들은 시차 주사 열량 측정법(DSC) 및 열중량 분석(TGA) 기술을 선택한다.
DSC: DSC는 재료로 들어오거나 재료에서 나가는 열류를 온도 또는 시간의 함수로 측정한다. 그래프 출력에서 볼 수 있는 상변화 발생 시 온도 변화와 흡수되거나 방출되는 열 사이의 열용량 관계가 중단된다. 안전한 작동 온도부터 열 남용까지의 다양한 조건에서 테스트할 수 있다.
TGA: TGA는 온도 또는 시간의 함수로 샘플의 질량을 측정한다. 일반적으로 말하자면, 열 안정성이 더 높은 재료는 더 높은 온도에 도달한 후에 질량 변화가 발생한다.
DSC의 결과로 다음 질문에 답하시오.
- 재료의 용융 온도, Tm
- 재료의 유리 전이 온도, Tg
- 배터리를 구성하는 다양한 재료의 가장 낮은 상변화 온도.
TGA의 결과로 다음 질문에 답하시오.
- 재료가 분해되기 시작하는 온도.
- 주어진 온도에서 열 분해 또는 산화 분해로 손실된 샘플 질량의 양.
- 주어진 온도에서 분해 반응(산화성 유도 분해와 열 유도 분해 모두 해당)의 속도.
- 배터리를 구성하는 다양한 재료의 최대 열 안정 온도.





