Mots clés : CDB, calorimétrie différentielle à balayage, batteries lithium-ion, emballement thermique, cathode, anode
TA467-FR
Résumé
L’emballement thermique qui survient dans les batteries lithium-ion est un problème de sécurité essentiel. Il se produit lorsque les matériaux des électrodes subissent des réactions exothermiques qui provoquent une augmentation de la température et une accélération de la cinétique des réactions. Il est établi que l’état de charge d’une batterie peut avoir un impact sur la température de déclenchement, le mécanisme et la libération d’énergie des réactions. La calorimétrie différentielle à balayage peut être utilisée pour évaluer la stabilité thermique des matériaux de la cathode et de l’anode à différents états de charge. La température de déclenchement des réactions ainsi que la température maximale de la réaction et l’énergie libérée peuvent être déterminées par le balayage des matériaux sur un intervalle de températures en utilisant la calorimétrie différentielle à balayage (CDB). Dans cette note, l’évaluation d’une cathode de lithium nickel manganèse cobalt (MMC) et d’une anode de graphite a permis d’observer une énergie de réaction supérieure dans la cathode, et une augmentation de la stabilité thermique lors de la diminution de l’état de charge.
Introduction
Les batteries lithium-ion (BLi) sont largement utilisées dans un grand nombre d’applications à cause de leurs propriétés, notamment une haute densité d’énergie. Des systèmes de gestion des batteries sont cependant nécessaires à cause des problèmes de sécurité soulevés par les BLi. Lorsqu’une batterie est en surcharge, exposée à des températures élevées ou en court-circuit, un emballement thermique peut se produire. L’échauffement jusqu’à une température critique entraîne des réactions exothermiques qui augmentent encore la température, et ne font qu’accélérer la cinétique de la réaction. Une dégradation catastrophique survient au cours de l’emballement thermique, ce qui provoque l’émission de gaz toxiques et la combustion de la batterie.
Il a été établi que l’état de charge (EdC) d’une BLi avait un impact direct sur l’emballement thermique. Des différences dans l’EdC modifient la configuration thermique de la cellule de la batterie, et le risque thermique est réduit chez les batteries qui présentent un EdC plus faible, dans la mesure où la réduction de la charge abaisse la libération potentielle d’énergie [1] [2]. Les matériaux utilisés dans la batterie affectent également l’emballement thermique. En outre, la connaissance des températures de déclenchement de l’emballement thermique pour différentes formulations et différents EdC est importante pour la conception de la gestion thermique et la prévention de l’emballement thermique.
La calorimétrie différentielle à balayage peut être utilisée pour mesurer le flux de chaleur des matériaux des électrodes. Un balayage sur un intervalle de températures permet de détecter les réactions exothermiques qui peuvent conduire à un emballement thermique. L’impact de l’EdC des matériaux sur la température de déclenchement et la quantité d’énergie libérée peut être mesuré, faisant de la calorimétrie différentielle à balayage un outil utile pour l’évaluation de la sécurité des batteries.
Données expérimentales
Des batteries à différents états de charge, munies d’une cathode NMC811 et d’une anode en graphite, ont été fournies par NEI Corporation. Avant le test, la batterie a été démontée et les électrodes lavées avec du diméthyl carbonate (DMC) pour retirer les électrolytes. Cette étape assure que les mesures évalueront uniquement les matériaux de la cathode et de l’anode, sans capturer la dégradation des électrolytes [3]. Après le séchage de l’électrode, les matériaux actifs de l’anode et de la cathode ont été retirés du collecteur actuel pour effectuer les tests. Afin d’effectuer une comparaison avec des échantillons chargés, les échantillons de la cathode et de l’anode tels qu’ils ont été reçus ont également été préparés en utilisant la même procédure de lavage et de séchage que les échantillons des états de charge.
Un calorimètre différentiel à balayage (CDB) de TA Instruments a été utilisé pour mesurer le flux de chaleur des matériaux des électrodes. Des échantillons d’environ 5 mg ont été chargés dans la nouvelle cuvette à haute température et haute pression (P/N 900803.901) et la température a été augmentée par paliers de 5 °C/min jusqu’à 450 °C. La température de déclenchement, la chaleur de la réaction (enthalpie) et la température maximale ont été analysées en utilisant le logiciel TRIOS.
Résultats et discussions
Les températures de déclenchement pour une cathode NMC et une anode en graphite entièrement chargées sont présentées sur la Figure 1. La première température de déclenchement, qui est le premier déplacement exothermique observé initialement, est souvent liée à la décomposition initiale de la couche d’interface électrolyte solide (IES), qui peut ensuite provoquer des réactions exothermiques indésirables. L’anode a une température de déclenchement inférieure de 82 °C, ce qui est typique des anodes en graphique habituelles. Les anodes en graphite montrent une décomposition initiale de l’IES comprise entre 80 °C et 120 °C [4].
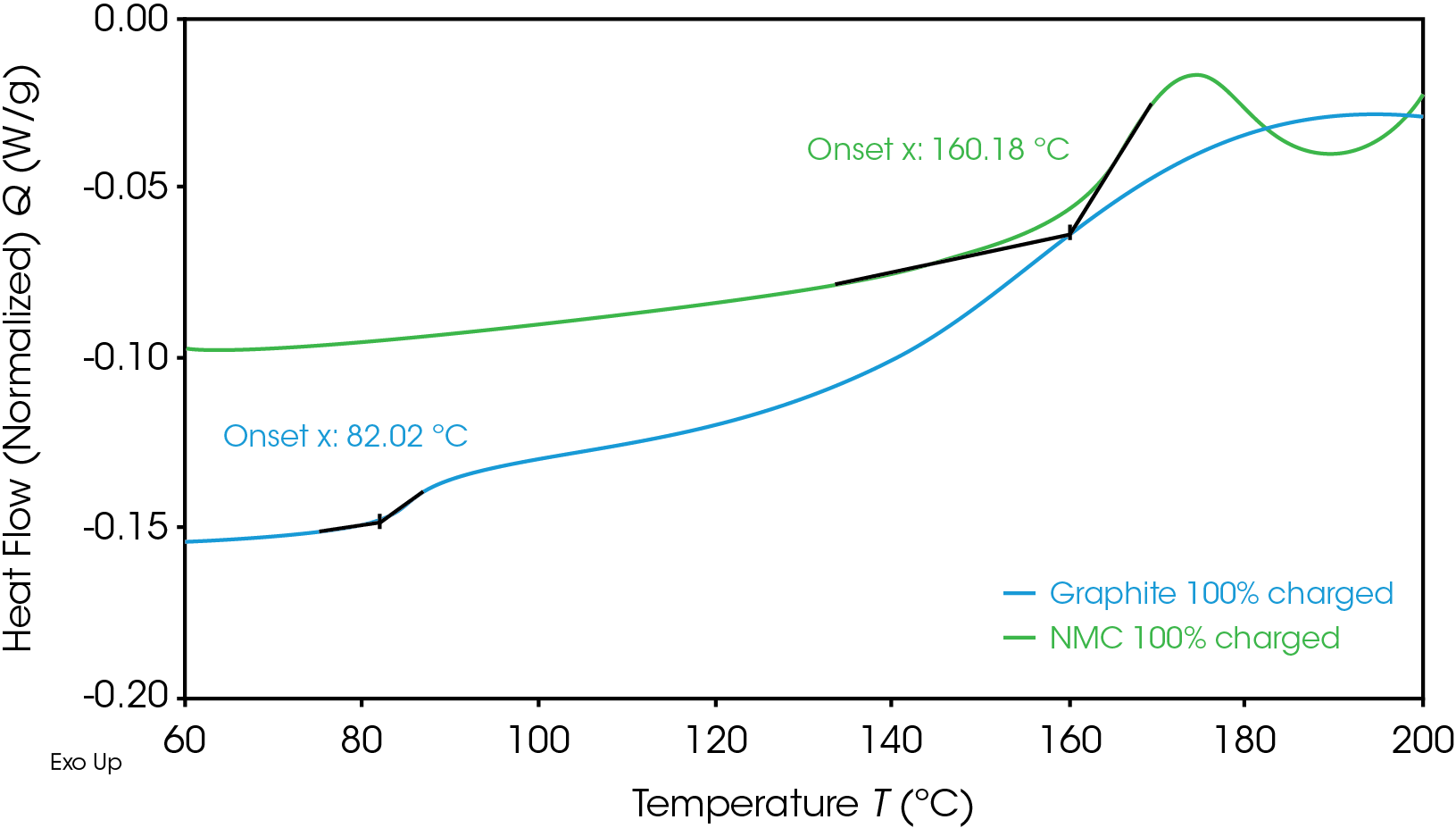
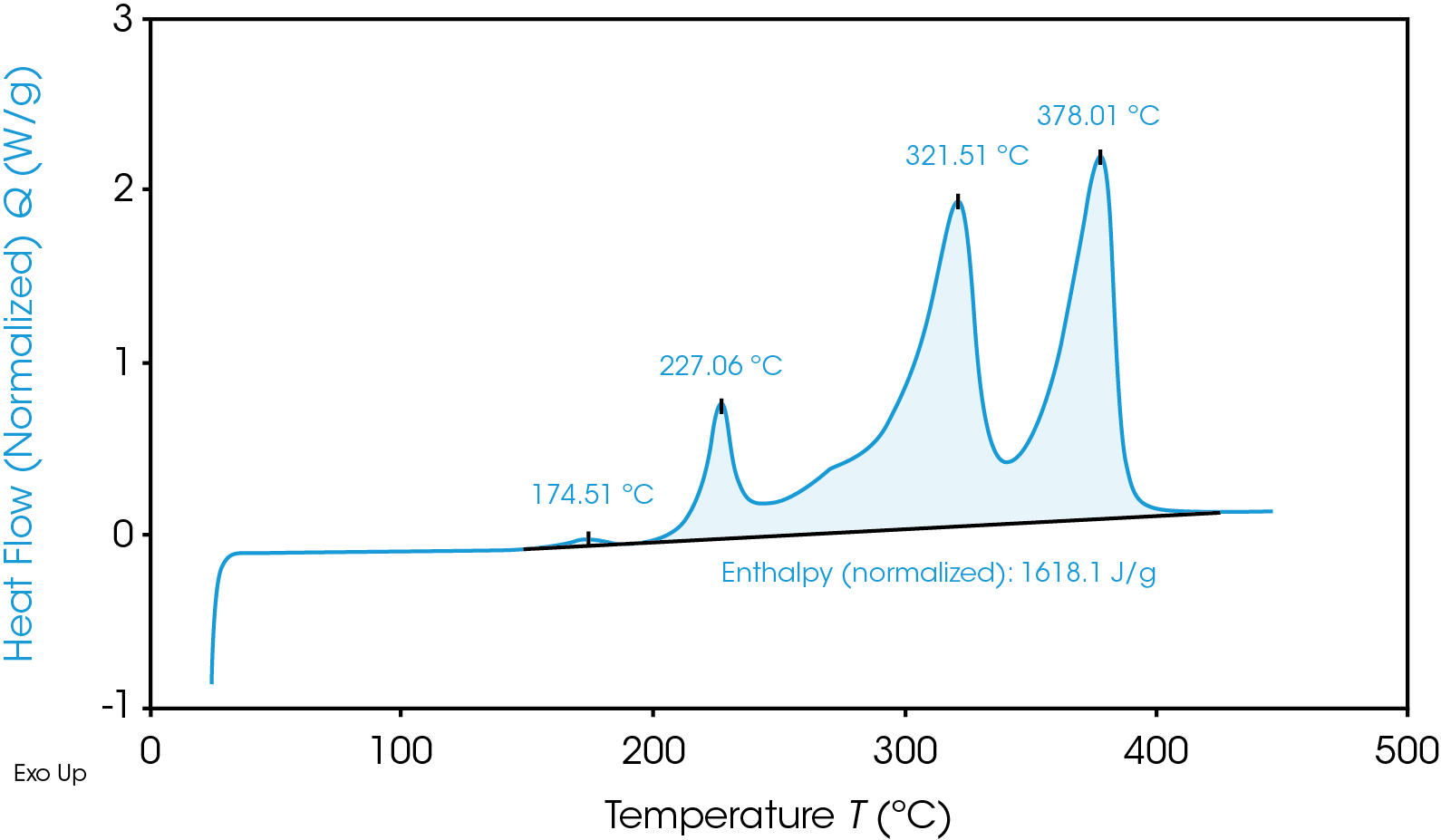
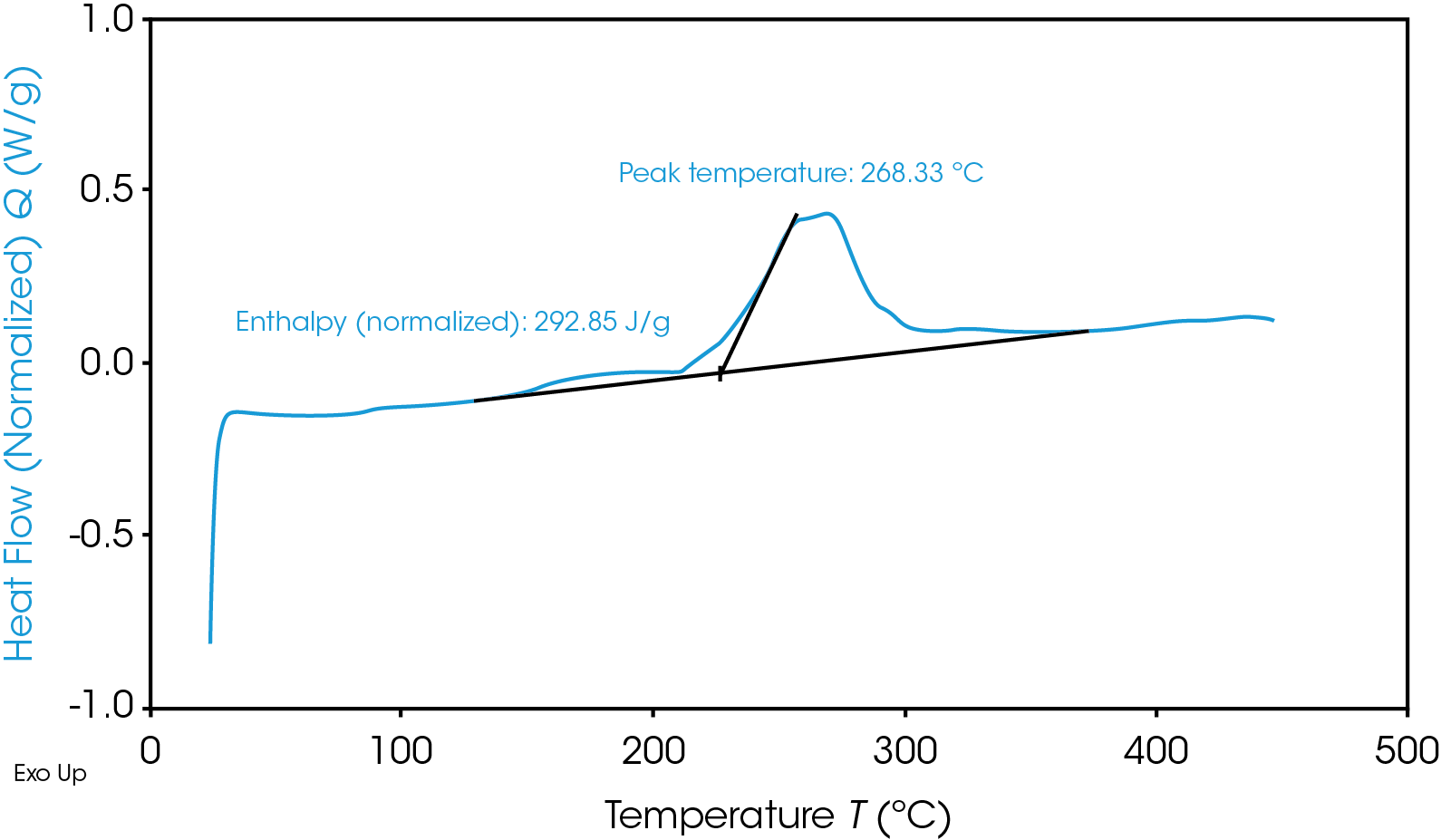
Bien que sa température de déclenchement soit inférieure, l’anode en graphite est globalement moins énergétique que la cathode NMC, comme le montre la Figure 2, avec une zone plus petite sous le signal du flux de chaleur du graphite. Cette zone correspond à l’enthalpie de la réaction, et peut être calculée par intégration de la courbe du signal du flux de chaleur. L’EdC à 100 % de la cathode NMC à une enthalpie de 1 618 J/g et l’enthalpie de l’anode de graphite à un EdC de 100 % est de 345 J/g. La cathode NMC à un EdC de 100 % présente davantage de réactions exothermiques énergétiques que l’anode de graphite à un EdC de 100 %. Les réactions exothermiques, liées à la dégradation des matériaux de la cathode, surviennent à 227 °C, 321 °C et 378 °C. Au-dessus de 270 °C, il est établi que l’alliage NMC devient thermiquement instable, et libère de l’oxygène [5] ; les pics de température de 321 °C et de 378 °C peuvent être liés à cette instabilité thermique. L’anode de graphite pleinement chargée provoque une réaction exothermique beaucoup plus faible à 268 °C. La libération d’énergie supérieure des réactions de la cathode est davantage susceptible de provoquer un emballement thermique et sa propagation à travers les batteries.
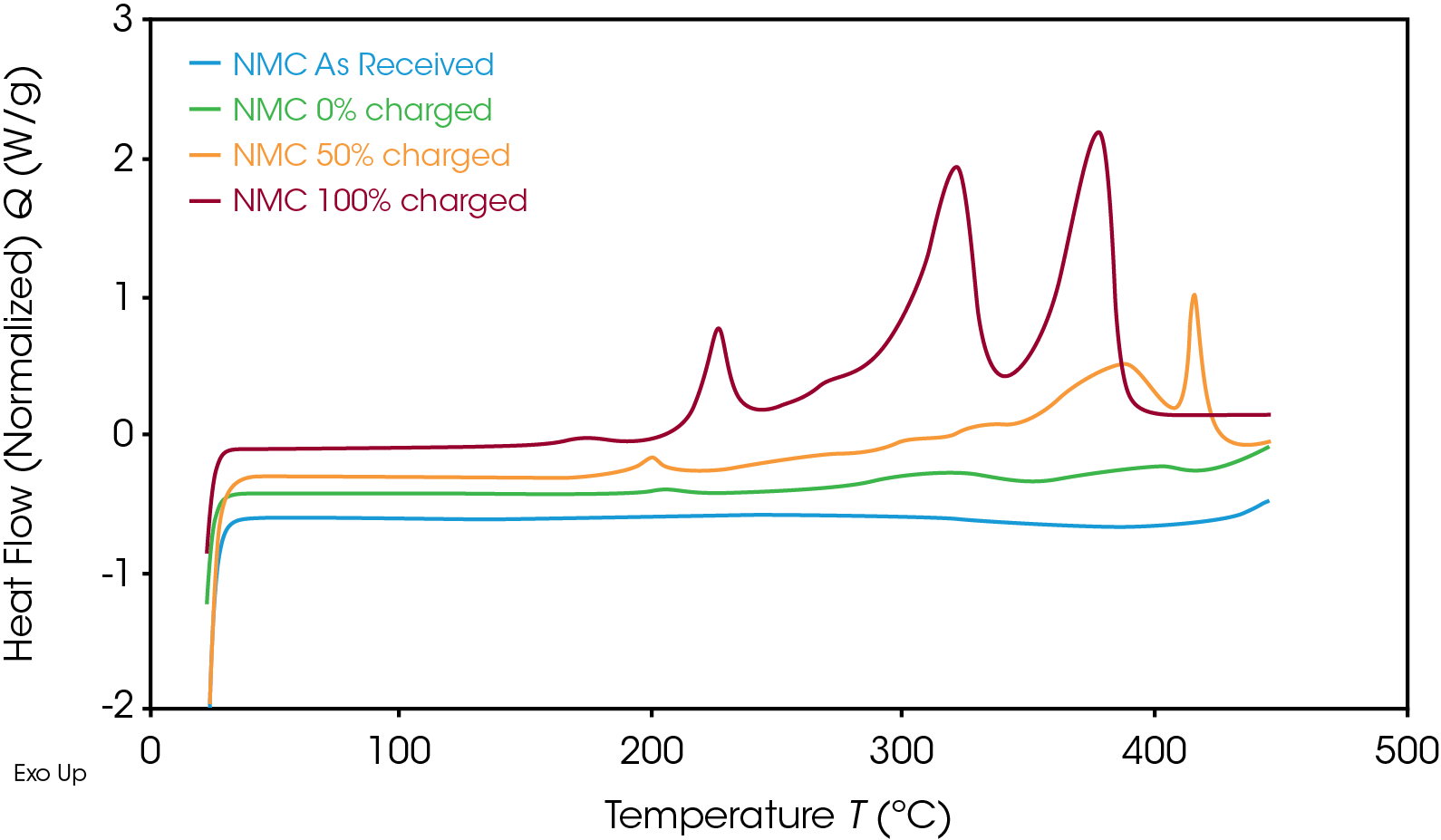
Le signal du flux de chaleur de la cathode NMC à différents EdC est présenté sur la Figure 3. La stabilité thermique augmente au fur et à mesure de la diminution de l’EdC. À un EDC de 50 %, le pic principal de l’événement exothermique est décalé de 378 °C à une température supérieure de 416 °C, et a libéré moins d’énergie qu’à un EdC de 100 %. Le matériau d’une cathode non chargée n’a présenté aucune réaction exothermique.
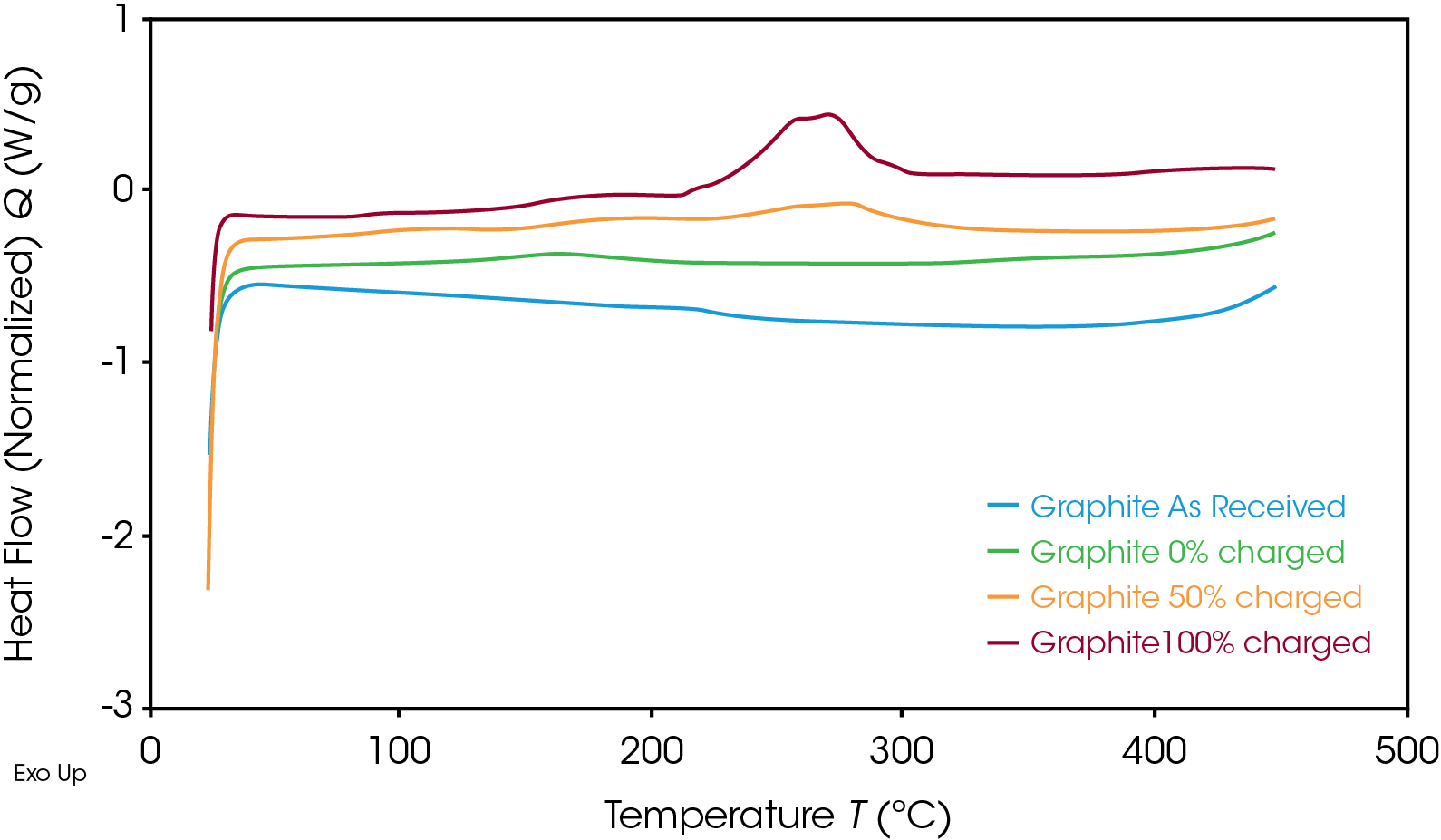
Comme attendu, l’anode a suivi la même tendance, comme le montre la Figure 4. Lorsque l’EdC de l’anode diminue, le flux de chaleur correspondant décroît également. La réaction exothermique à libérer moins d’énergie à un EdC de 50 % qu’à un EdC de 100 %. L’enthalpie par unité de masse pour les deux matériaux à différents EdC est présentée dans le Tableau 1.
Table 1. Enthalpy of reactions at various SOC for the NMC cathode and graphite anode
| Enthalpy (J/g) | Cathode NMC | Anode en graphite |
|---|---|---|
| 0% SOC | 72.1 | 49.8 |
| 50% SOC | 625 | 216 |
| 100% SOC | 1618 | 345 |
Lorsqu’elles ne sont pas chargées, l’enthalpie de la réaction pour l’anode en graphite et la cathode NMC est similaire. Cependant, pour cette batterie, l’énergie libérée dans l’anode de graphite chargée est significativement inférieure à celle de la cathode NMC chargée, ce qui montre que la cathode présente un risque supérieur de provoquer un emballement thermique. La cathode pleinement chargée libère plus de trois fois plus d’énergie qu’une anode pleinement chargée pour cette batterie ; cette libération d’énergie risque davantage d’entraîner dans la batterie des réactions susceptibles de provoquer un emballement thermique. Il est important que les deux électrodes soient étudiées afin de déterminer quels matériaux présentent les facteurs de risque les plus élevés et quelles températures doivent être évitées. La batterie en pleine charge doit rester à un niveau inférieur à la température de déclenchement afin d’éviter une dégradation et une instabilité thermique dangereuses. Les résultats de la CDB contribuent à la conception de systèmes de gestion thermique grâce à la compréhension des paramètres de sécurité des matériaux des batteries.
Conclusions
La CDB peut être utilisée pour l’analyse de la sécurité des matériaux des électrodes vis-à-vis du risque d’emballement thermique. La température des réactions qui sont susceptibles de provoquer un emballement thermique peut être déterminée, ainsi que la quantité d’énergie libérée au cours des réactions de dégradation. Les électrodes à différents EdC (100 %, 50 %, 0 %) ont été analysées, une cathode NMC à un EdC de 100 % présentant le risque maximal d’emballement thermique et de propagation à travers les batteries. Lorsque l’EdC est réduit à 50 %, la cathode NMC devient thermiquement plus stable, avec un décalage de la réaction exothermique à une température plus élevée. L’anode de graphite, tout en suivant la même tendance concernant l’edC, libère significativement moins d’énergie que la cathode.
Références
- L. Torres-Castro, A. Kurzawski, J. Hewson and J. Lamb, “Passive mitgation of cascading propagation in multi-cell lithium ion batteries,” Journal of the Electrochemical Society, vol. 167, no. 9, 2020.
- A. W. Golubkov, S. Scheikl, R. Planteu, G. Voitic, H. Wiltsche, C. Stangl, G. Fauler, A. Thaler and V. Hacker, “Thermal runaway of commercial 18650 Li-ion batteries with LFP and NCA cathodes- impact of state of charge and overcharge,” RSC Advances, vol. 5, pp. 57171-57186, 2015.
- Z. Zhang, D. Fouchard and J. R. Rea, “Differential scanning calorimetry material studies: implications for the safety of lithium-ion cells,” Journal of Power Sources, vol. 70, pp. 16-20, 1998.
- X. Feng, M. Ouyang, X. Liu, L. Lu, Y. Xia and X. He, “Thermal runaway mechanism of lithium ion battery for electric vehicles :A review,” Energy Storage Materials, vol. 10, pp. 246-267, 2018.
- K. Kim, D. Kam, C. C. Nguyen, S.-W. Song and R. Kostecki, “Study on the Dominant Film-Forming Site Among Components of Li(Ni1/3Co1/3Mn1/3)O2 Cathode in Li-ion Batteries,” Bulletin of the Korean Chemical Society, vol. 32, no. 8, 2011.
Remerciements
Cette note a été conçue en collaboration entre NEI Corporation (Somerset, New Jersey) et TA Instruments. Elle a été rédigée par Jennifer Vail, PhD et Hang Lau, PhD, directeur scientifique du développement des nouveaux marchés à TA Instruments.
Cliquez ici pour télécharger la version imprimable de cette note d’application.

